Urutan Keelektronegatifan Dari Unsur 11na 19k Dan 37rb – Hal ini dapat menyebabkan: 1) Pada periode di mana kerapatan atom meningkat dari atas ke bawah 2) Pada periode di mana kerapatan atom menurun dari kiri ke kanan 1. Diketahui unsur: 3Li, 4Be, 5B, 9F. Rumus : unsur dengan massa atom terbesar 2. Unsur yang diketahui : 11Na, 19K, 37Rb, 55Cs Rumus : unsur dengan massa atom terbesar 2. Energi ionisasi Energi energi yang diperlukan untuk melepaskan elektron terluar suatu atom. Kekuatan ionik ini dinyatakan dalam satuan kJ mol-1. Untuk unsur-unsur dalam golongan, energi ionisasi menurun sepanjang garis karena elektron terluar lebih jauh dari inti (daya tarik inti lebih lemah), sehingga elektron terluar lebih jauh dari inti. rilis lebih banyak 11 Fungsi Individu
Sedangkan untuk unsur-unsur dengan periode yang sama, gaya gravitasinya ke kanan, yang berarti gaya ionisasi biasanya lebih ke kanan. Ada beberapa pengecualian yang perlu diperhatikan. Golongan IIA, VA dan VIIIA memiliki energi ionisasi yang sangat tinggi, lebih besar dari energi ionisasi unsur-unsur di sebelah kanannya, seperti IIIA dan VIA. Apakah karena unsur golongan IIA, VA, dan VIIIA memiliki muatan listrik yang tetap, sehingga sulit untuk melepaskan listrik dalam jangka waktu tertentu?3. Keelektronegatifan Keelektronegatifan adalah kemampuan atau kecenderungan suatu atom untuk memperoleh atau menarik elektron dari atom lain. Misalnya, fluor cenderung menarik elektron lebih kuat daripada hidrogen. Oleh karena itu, dapat disimpulkan bahwa keelektronegatifan fluor lebih besar daripada hidrogen. Konsep keelektronegatifan pertama kali dikemukakan oleh Linus Pauling (190112. Lihat bagan di bawah ini. Karya Individu
Urutan Keelektronegatifan Dari Unsur 11na 19k Dan 37rb
– 1994) pada tahun 1932. Unsur-unsur dari golongan yang sama, keelektronegatifannya semakin kecil karena tarikan inti semakin lemah. Sedangkan untuk unsur-unsur yang berada pada periode yang sama, keelektronegatifan di sebelah kanan lebih besar. Namun, harus diingat bahwa golongan VIIIA tidak memiliki keelektronegatifan. Ini karena sudah memiliki 8 elektron di kulit terluarnya. Jadi, tingkat keelektronegatifan golongan VIIA Berdasarkan Tabel 1.4, 1. Berapakah tingkat keelektronegatifan unsur-unsur pada: a. bagian (dari atas ke bawah) b. periode (dari kiri ke kanan) 2. Elemen populer: 19K, 20Ca, 31Ga, 36Kr. Yang meliputi: a. keelektronegatifan tinggi?b. kurang elektronegativitas?3. Elemen populer: 9F, 17Cl, 35Br, 53I. Yang meliputi: a. keelektronegatifan tinggi?b. kurang elektronegativitas?4. Afinitas elektron Afinitas elektron adalah energi yang menyertai proses penambahan 1 elektron ke atom netral dalam keadaan gas, menghasilkan ion bermuatan -1. Afinitas elektron juga ditunjukkan dalam kJmol-1. Unsur yang memiliki muatan negatif. artinya, mereka lebih berarti
Diketahui Unsur Unsur: 19k, 20ca, 31ga, 36kr. Manakah Yang Memiliki:a. Keeletronegatifan
30. Suhu ideal untuk memelihara Whitefish adalah… A. 26-29°C B. 27-30°C. 28-32°C D. 29-33°C.
Amonia mengandung 17,65% H dan 82,35% N. Jika 5,29 g hidrogen bereaksi dengan 24,71 gram nitrogen, akan dihasilkan 30,0 g amonia. Tunjukkan data… itu mematuhi hukum proporsionalitas!.
Diketahui bahwa KCIO3 + 3Mg KCl + 3MgO AH = – 1852 kJK+ 1/2 Cl2 + 3/2 02 →KCIO3 AH = -391 kJAH KCl = -437 kJ/mol Entalpi standar pembakaran Mg. KJ/mol(… A) – 1204(B) – 602(C) -301(D) – 60,2(E) – 30,1.
Sekitar 39 gram kalium direaksikan dengan 200 mL HCl 5 M untuk menghasilkan kalium klorida dan gas hidrogen (H2). Penalaran: a. Massa gas hidrogen b. Volume larutan kalsium klorida yang dihasilkan pada kondisi normal.A. Bagian IA, periode 4 B. Bagian IA, periode 5 C. Bagian II A, periode 5 D. Bagian VII A, periode 4 E. Bagian VIII A, periode 5
Diketahui Unsur Unsur 11na, 12mg, 16s, 17cl Dan 19k. Pern
3. Pasangan unsur dalam satu periode adalah unsur dengan nomor atom… A. 2 dan 3 B. 1 dan 11 C. 12 dan 17 D. 36 dan 37 E. 18 dan 19
4. Kalsium memiliki nomor atom 20. Dalam tabel periodik unsur, kalsium berada dalam golongan….dan periode….. A. IIA dan 4 B. IIA dan 5 C. IIIA dan 4 D PPN dan 5 E.VA dan 3
A. Dalam satu periode dari kiri ke kanan unsur bukan logam bertambah B. Dalam satu periode dari kiri ke kanan nomor atom bertambah C. Dalam periode dari kiri ke kanan berat atom bertambah D. Dalam golongan dari atas ke bawah unsur logam sifat meningkat. E Dalam golongan dari atas ke bawah energi ionisasi bertambah
7. Energi ionisasi unsur Li, Na, K, Rb, dan Cs menurun. Faktor utama yang menyebabkan berkurangnya energi ionisasi adalah bertambahnya… A. Konsentrasi B. Muatan nuklir C. Jari-jari atom D. Massa atom E. Nomor atom
Bab 1 Struktur Atom Dan Sistem Periodik Unsur Kata Kunci Pengantar Pages 1 44
9 8. Hasil klasifikasi unsur berdasarkan sifat fisika dan kimia yang berkaitan dengan massa atom unsur disusun oleh A. Dobereiner B. D.I. Mendeleev C. Henry G.J. Moseley D. John Newlands E. Lothar Meyer
9. Suatu unsur memiliki keelektronegatifan Unsur berada dalam golongan …… A. IA B. VA C. VIA D. VIIA E. VIIIA
10. Unsur Sn memiliki keelektronegatifan Unsur berada pada periode …. A. 3 B. 4 C. 5 D. 6 E. 7
12 11. Suatu atom terletak pada golongan III A periode 4, maka konfigurasi elektron unsur tersebut adalah A B C D E.
Kumpulan Contoh Soal Tabel Periodik Dan Sifat Keperiodikan Unsur
A. afinitas elektron rendah B. energi ionisasi tinggi C. nomor atom kecil D. kecenderungan membentuk ion positif E. gaya atom besar
A. tergolong nonlogam B. membentuk molekul diatomik C. memiliki 7 elektron valensi D. termasuk golongan VI A E. dapat bereaksi dengan logam membentuk garam.
17. Jika x dan y adalah pasangan unsur dengan elektron valensi yang sama, maka nomor atom x dan y adalah … A. 11 dan 20 B. 15 dan 32 C. 12 dan 20 D. 17 dan 34 E. 13 dan 18
A. Dari atas ke bawah dalam suatu golongan energi ionisasi bertambah B. Dari atas ke bawah dalam suatu golongan jari-jari atom bertambah C. Dari atas ke bawah dalam suatu golongan keelektronegatifan berkurang D. Dari kiri ke kanan dalam satu periode kedekatan elektron b . masing-masing berukuran E. Dari kiri ke kanan seiring waktu nomor atom menjadi semakin kecil.
Diketahui Unsur Unsur: 11na, 19 K, 37rb, 55cs. Tentukan:
21 20. Suatu unsur dalam SPU terletak pada golongan VA dan periode 3, karena nomor atom unsur tersebut adalah … A. 3 B. 5 C. 10 D. 15 E. 20
A. penurunan kerapatan elektron B. penurunan kerapatan elektron C. peningkatan energi ionisasi D. penurunan kerapatan elektron E. peningkatan kerapatan elektron .
24. Unsur X mempunyai 16 neutron, nomor massanya 31. Unsur dalam SPU modern berada pada golongan …… periode ……. A. VA , 3 B. VI A, 3 C.III A, 4 D.IV A, 4 E.I.A, 4
25. Nomor atom unsur = 58 dan nomor massa = 140. Karena jumlah elektron, proton dan neutron adalah … A. 58, 24, 58 B. 58, 82, 58 C. 58 , 58, 24 D 58, 58, 140 E. 58, 58, 82
Diketahui Unsur 9 F , 17 Cl , 35 Br Dan 53 I . Urutkan Da
Untuk mengoperasikan situs web ini, kami merekam data pengguna dan membaginya dengan pabrikan. Untuk menggunakan situs web ini, Anda harus menerima Kebijakan Privasi kami, termasuk kebijakan cookie kami. 10 unsur teratas di antara 11 unsur 12 mg 19 k 20 ca 37 k memiliki jari-jari atom terbesar tahun 2022
Top 1 : Diantara unsur 11Na, 12Mg, 19K, 20Ca dan 37Rb… – Mas Dayat. Top 1: Di antara unsur-unsur 11Na, 12Mg, 19K, 20Ca, 13A1 ada…
Ringkasan: . Hitung molalitas larutan glukosa 12% dengan berat glukosa Mr=180 . hitung molalitas larutan yang mengandung 9 gram glukosa mr = 180 dilarutkan dalam 500 gram air. Berapa jumlah atom Na²Cr²O². jika ada NaoH (1,5 molal), MR NaoH = 40, hitung molaritas HaoH. Berikan gambaran umum tentang contoh aplikasi kimia hijau di lingkungan. Peran kimia di berbagai bidang. hitunglah volume larutan di dalamnya
Cocokkan hasil analisis: Jadi, kekuatan ion maksimum: bagian terbesar (atas) dan periode terkecil (kanan). Dari susunan di atas terlihat bahwa kelompok terbesar adalah……
Diketahui Unsur 11na 13 Al 19k 37rb Urutkan Unsur Unsur Berdasarkan Kenaikan Jari Jari Atom Dan
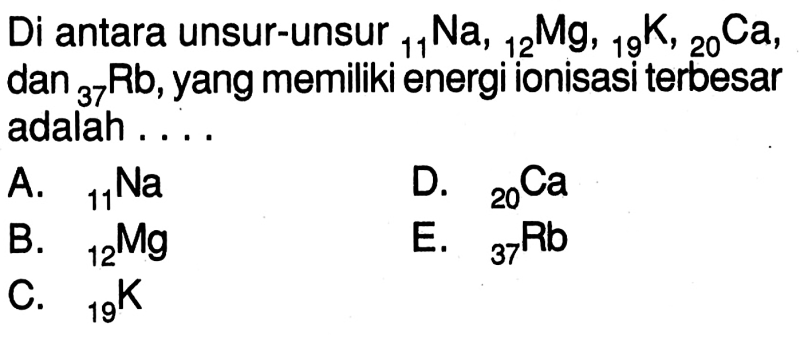
Ringkasan: . . Diantara unsur 11Na, 12Mg, 19K, 20Ca dan 37Rb, yang memiliki energi ionisasi tertinggi adalah … A.11Na B.12Mg C.19K D.20Ca E.37Rb Debat:11Na = 2. 8. 1 (periode IA 3)12Mg = 2 . 8. 2 (bagian IIA 3)19K = 2 . 8. 8. 1 (periode IA 4)20Ca = 2 . 8. 8. 2
Contoh penelitian: 2 Juli 2021 — Di antara unsur-unsur 11Na, 12Mg, 19K, 20Ca, dan 37Rb, unsur dengan energi ionisasi tertinggi adalah… A. 11Na. B.12Mg. C.19K. D.20 Tentang. …
Ringkasan: Di antara unsur-unsur 11Na, 12Mg, 19K, 20Ca, 13Al yang memiliki energi ionisasi tertinggi adalah ₁₃Al [yang memiliki jari-jari atom terkecil]. Ini karena unsur yang tidak stabil mudah bereaksi dengan unsur lain. Reaktivitas suatu unsur tergantung pada jari-jari atomnya, kekuatan ionisasi, ikatan listrik dan elektroniknya. Nilai standar dalam tabel misalnya
Hasil uji kecocokan: 18 Mei 2022 — Di antara unsur-unsur 11Na, 12Mg, 19K, 20Ca, 13Al dengan energi ionisasi tertinggi adalah ₁₃Al jari-jari atom … …
Tentukan Jari Jari Atom Dari Terkecil Ke Yang Terbesar Dari Unsur 37rb, 55cs, 87fr …
Ringkasan: Konfigurasi elektron unsur Menurut konfigurasi elektronnya, unsur Na berada pada golongan I A dan periode 3 Konfigurasi elektron unsur Menurut konfigurasi elektronnya, unsur Mg berada pada golongan II A dan periode 3 Konfigurasi elektron unsur. Berdasarkan konfigurasi kelistrikannya, unsur K berada pada golongan I A dan periode 4 Konfigurasi kelistrikan unsur Berdasarkan konfigurasi kelistrikannya, unsur Ca berada pada golongan II A dan periode 4 Konfigurasi kelistrikan unsur.
Hasil analisis yang sesuai: Energi ionisasi adalah energi yang dibutuhkan untuk melepaskan elektron. Dalam satu periode, dari kiri ke kanan adalah nilai energi ionisasi tertinggi. Dalam……
Ringkasan: Konfigurasi Elektron Unsur Menurut konfigurasi elektronnya, unsur Na pada golongan I A dan periode 3 Konfigurasi Elektron Unsur.
Urutan shio dan unsur, jenis pupuk organik untuk menambah dan melengkapi kandungan unsur hara yang kurang dari tanah adalah, atom unsur 19k akan menjadi stabil dengan kecenderungan, tuliskan lambang dari unsur hidrogen oksigen dan belerang, urutan giling kopi dari halus dan kasar, unsur estetika dan ergonomis produk kerajinan dari bahan lunak





Leave a Comment